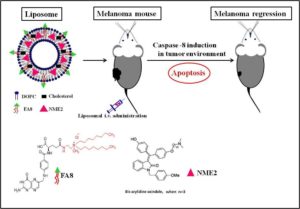
在癌症中,肿瘤的快速生长归因于抗凋亡蛋白的过度表达,凋亡蛋白酶如半胱天冬酶的抑制或功能低下。半胱氨酸天冬氨酸酶caspase-8信号级联是非常重要和有趣的,因为它能够通过线粒体介导的内源性和死亡受体介导的外源性途径诱导细胞死亡。尤其是,在卵巢癌患者中,低水平半胱天冬酶8的肿瘤对化疗具有内在的抵抗力。顺便说一下,侵袭性黑色素瘤细胞在细胞膜上具有叶酸受体(fr)和细胞质中雌激素受体(er)的功能性表达。把这些基本事实结合起来,人们就可以提供抗癌药物,可能是瞄准机,利用脂质体系统携带fr靶向配体治疗侵袭性黑色素瘤细胞。
在目前的工作中,班纳吉集团使用一种叫做nme2的疏水性药物分子(一种最近开发的用于治疗乳腺癌的ER靶向抗癌药物)。使用特殊的fr靶向脂质体,该药物成功地输送到中度表达的fr黑色素瘤细胞。
一种新的功能强大的靶向适度表达的fr黑色素瘤细胞的方法是成功的。阳离子叶酸配体命名为fa8。这种传递效率与其他靶向fr的脂质体形成鲜明对比,后者仅靶向fr过度表达的癌细胞。fa8相关脂质体中nme2的合成选择性诱导caspase-8表达介导黑色素瘤细胞凋亡(体外和体内)然而,未经靶向脂质体或未经靶向脂质体处理的药物均不能诱导caspase-8介导的细胞凋亡。初步地,多西他赛,另一种有效的抗癌药物,在FA8介导的分娩中也显示了类似的结果。显然,给定的fr目标,脂质体传递方法表明药物货物的抗癌作用机制发生了变化,因此证明了一种有趣的可能性,即可以避免对给定药物的耐药性(如果有的话)。
作者提示:
1)在MDR癌症中,重新利用药物的机械途径至关重要,获得性耐药性是癌症治疗的主要障碍之一。
2)给定的fr靶向制剂影响了药物货物作用机制的变化(此处,nme2)从非caspase 8到caspase-8介导的凋亡,从而重新利用胶囊药物的凋亡途径。
3)独特的阳离子脂质结合叶酸配体促进a)靶向fr中度表达的黑色素瘤细胞;b)修改药品货物的机械作用。
4)具有fr靶向配体的脂质体传递系统通过caspase-8的上调以及随后的促生存因子rip-1的分裂,激活了一个独立的细胞死亡途径。
文章链接:
阳离子叶酸介导的双芳环内酯-氧化吲哚脂质体传递诱导黑色素瘤肿瘤的有效消退 生物活性剂SCI。,2017,五,1898-199
关于Webwriter:
 博士。Sudip Mukherjee是生物材料科学新利手机客户端.他目前是博士后研究助理,与博士一起工作。米斯大学生物工程系的奥米德韦瑟。他的研究涉及开发先进的纳米材料用于癌症治疗中的药物/基因传递,免疫调节应用与血管生成。他总共发表了约30篇研究文章/专利。他担任国际咨询委员会成员材料研究快报‘,眼科科学新利手机客户端他是英国皇家化学学会的准会员。新利手机客户端英国。他是几家国际期刊的审稿人,如化学硕士作者:作者:生物医学纳米技术杂志,RSC进展,IOP纳米技术等。
博士。Sudip Mukherjee是生物材料科学新利手机客户端.他目前是博士后研究助理,与博士一起工作。米斯大学生物工程系的奥米德韦瑟。他的研究涉及开发先进的纳米材料用于癌症治疗中的药物/基因传递,免疫调节应用与血管生成。他总共发表了约30篇研究文章/专利。他担任国际咨询委员会成员材料研究快报‘,眼科科学新利手机客户端他是英国皇家化学学会的准会员。新利手机客户端英国。他是几家国际期刊的审稿人,如化学硕士作者:作者:生物医学纳米技术杂志,RSC进展,IOP纳米技术等。