随着纳米医学的迅速发展,无毒的,可生物降解的靶向纳米载体,能够封装活性药物或生物分子,并能在靶点实现有效载荷的可控释放,已成为更灵敏、准确诊断和更有效治疗的新型治疗工具。通过我们对疾病和当前纳米载体的影响的不断了解,朝着进一步增强和智能化的方向发展,刺激反应聚合物是微不足道的。然而,以生殖和控制的方式设计这种材料并非毫无挑战。因此,新的合成方法和方案,可获得最佳尺寸和形状的多组分纳米载体,可接受疾病病理学和生物化学,且完全无毒。新利手机客户端可生物降解,并允许有针对性的分配是非常及时的。
皮拉达什维利等最近在纳米尺度层一种有效但简单的纳米载体的制备血浆稳定并且是酶降解.为了他们的准备,光触发和无催化剂四唑烯环加成(tet-click)对生物降解天然聚合物,获得人血清白蛋白(HSA)。弗斯特,tet通过steglich酰胺化与hsa结合;和第二;利用TET-HSA在油包水微乳液中的面间交联反应,在254nm紫外光照射下获得稳定的荧光水性纳米载体。(图1)。
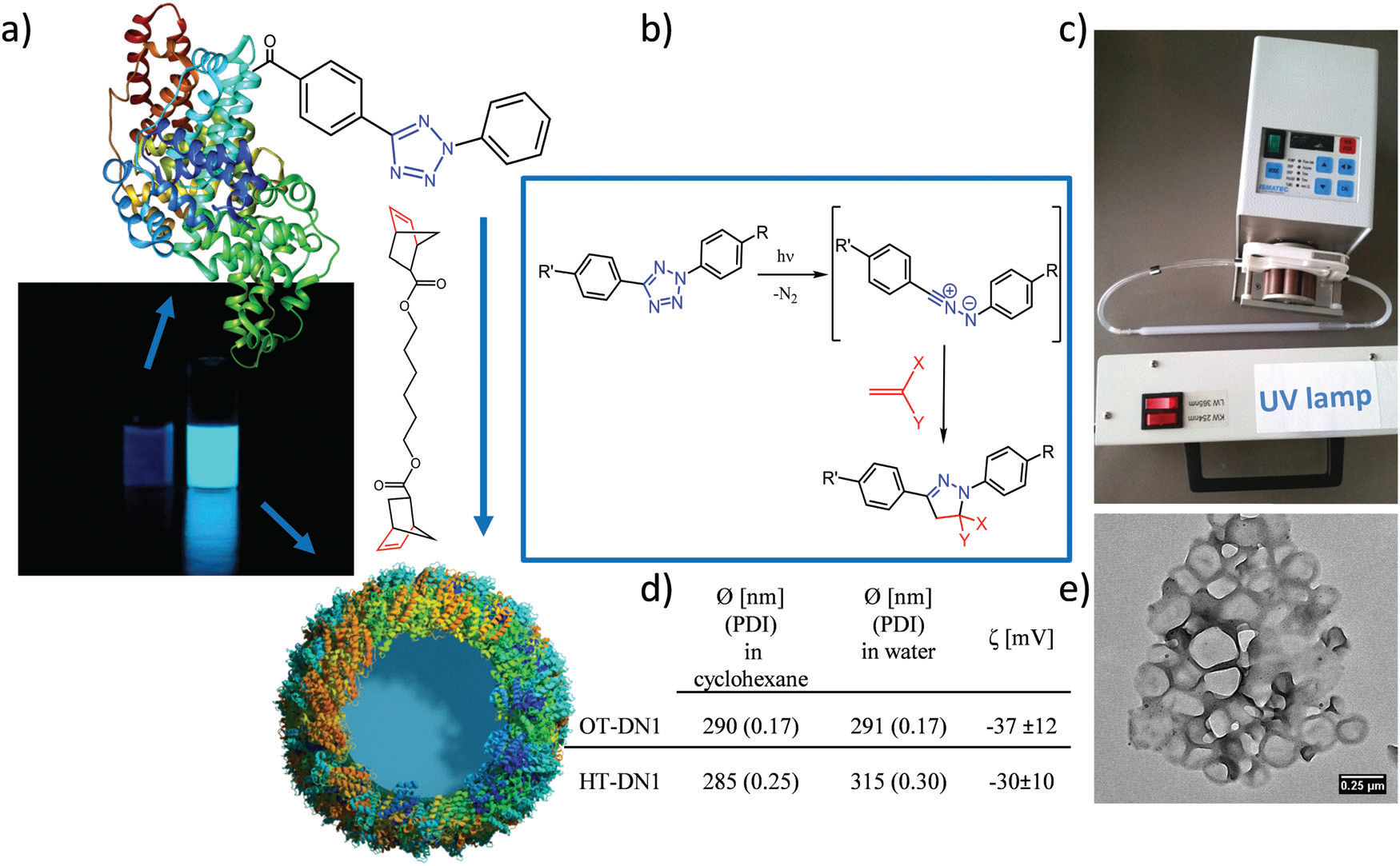 图1。蛋白质纳米载体的制备。(a)非荧光蛋白-tet结合物经二诺伯尼反相微乳液交联,得到自荧光蛋白纳米载体;(b)生物正交紫外光诱导1,3偶极四唑烯环加成反应机理;(c)用蠕动泵将乳状液泵入石英试管并将紫外线灯置于前面的实验装置;(d)各种蛋白质纳米载体的平均尺寸;(e)蛋白质纳米载体的透射电镜图像。经英国皇家化学学会许可复制的图像。新利手机客户端
图1。蛋白质纳米载体的制备。(a)非荧光蛋白-tet结合物经二诺伯尼反相微乳液交联,得到自荧光蛋白纳米载体;(b)生物正交紫外光诱导1,3偶极四唑烯环加成反应机理;(c)用蠕动泵将乳状液泵入石英试管并将紫外线灯置于前面的实验装置;(d)各种蛋白质纳米载体的平均尺寸;(e)蛋白质纳米载体的透射电镜图像。经英国皇家化学学会许可复制的图像。新利手机客户端
合成的纳米载体被证明封装了一个高药物有效载荷(R848)的超过90%.此外,将封装的R848纳米载体高度内化到衍生树突状细胞(BMDC)中并以功能性方式释放。以及非常稳定。有没有聚集或退化的迹象,甚至在CA之后。储存8个月,因此没有发生R848泄漏。
这种方法可以作为一个平台,设计各种各样的蛋白质封装。这种纳米疗法的临床翻译还需要进一步的临床前和临床试验。尽管如此,本文报道的有效方法可以在纳米疗法的进化和革命道路上发挥关键作用。
博士。奥尔扎是的成员纳米水平社区委员会.她是埃默里医学院纳米医学实验室的高级研究科学家,美国。她完成了博士学位。关于化学系治疗性纳米颗粒的发展,新利手机客户端利物浦大学英国博莱雅宝贝大学,罗马尼亚。她的研究重点是为生物医学应用开发混合工程纳米材料,例如:组织工程和癌症治疗/诊断。这种纳米材料的创新设计方法来自化学,新利手机客户端生物技术,生物学/医学,和工程。此外,博士。Orza是Indagomed公司的董事兼首席科学家。LLC美国一家专注于通过纳米技术创造高性能产品的公司。